
|
Ответы к упражнениям § 8. Химия 9 класс.
|
Упражнение: 1
 Определите
число электронов, которое отдают три атома железа молекуле воды в
реакции образования железной окалины Определите
число электронов, которое отдают три атома железа молекуле воды в
реакции образования железной окалины
|
 3Fe + 4 H2O = Fe3O4
+ 4H2O ↑ 3Fe + 4 H2O = Fe3O4
+ 4H2O ↑
т. к. Fe3O4 - это смесь 2 оксидов:
Fe3O4 = FeO • Fe2O3, то реакцию
можно записать так:
3Fe0
+ 4 H2O = Fe+2O
• Fe2+3O3 + 4H2O ↑
Fe0 -2e → Fe+2
2Fe0 -6e → 2Fe+3
3Fe0 -8e → Fe+2 + 2Fe+3
Ответ: 8 электронов отдают атомы железа в данной реакции.
|
Упражнение: 2
 Вычислите объем воздуха (н.у.), который потребуется для сжигания 36 г
магния. (Напоминаем, что объемная доля кислорода в воздухе равна 0,21.)
Вычислите объем воздуха (н.у.), который потребуется для сжигания 36 г
магния. (Напоминаем, что объемная доля кислорода в воздухе равна 0,21.)

Дано:
Mg, O2
m(Mg) =
36 г
φ(O2) =
0,21
Vвозд. =?
|
Решение:

36 : 48 = х : 22,4 х = 16,8 л кислорода
(О2)
В 100 л возд. содержится 21 л. О2
В х л. возд. содерхится 16,8 л. О2
21 • х = 100 • 16,8 х = 80 л. воздуха
Ответ: для сжигания 36 г. магния
необходимо 80 л. воздуха. |
|
Упражнение: 3
 Вычислите
объем водорода (н.у.), который может быть получен при растворении в
воде 120 мг кальция, если выход газа составит 80% от теоретически
возможного. Вычислите
объем водорода (н.у.), который может быть получен при растворении в
воде 120 мг кальция, если выход газа составит 80% от теоретически
возможного.

Дано:
Ca, H2O
m(Ca) = 120 мг
W(H2) = 0,8
V(H2) =?
|
Решение:

120 : 40 = х : 22.4 х = 67,2 мл. - теоретический оъем водорода Vтеор.(H2)
Vпр.(H2) • W(H2) • Vтеор.(H2)
Vпр.(H2) = 0,8 • 67,2 = 53,76 мл - практический объем водорода
Ответ: V(H2) = 53,76 мл
. |
|
Упражнение: 4
 Почему щелочные и щелочноземельные металлы хранят под керосином. Почему литий, в отличие от натрия и калия хранят в вазелине?
Почему щелочные и щелочноземельные металлы хранят под керосином. Почему литий, в отличие от натрия и калия хранят в вазелине?
 Щелочные
и щелочноземельные металлы хранят под слоем керосина, так как на
воздухе они активно взаимодействуют с кислородом воздуха. Литий хранят
в вазелине из-за его малой плотности - он всплывает в керосине Щелочные
и щелочноземельные металлы хранят под слоем керосина, так как на
воздухе они активно взаимодействуют с кислородом воздуха. Литий хранят
в вазелине из-за его малой плотности - он всплывает в керосине
|
Упражнение: 5
 Методом электронного баланса определите коэффициенты в уравнении реакции, схема которого:
Методом электронного баланса определите коэффициенты в уравнении реакции, схема которого:
Ca + HNO3 → Ca(NO3)2 + N2↑ + H2O
Какой ион проявляет в этой реакции окислительные свойства?


|
Упражнение: 6
 Можно ли получить водород при взаимодействии свинца с раствором серной кислоты?
Можно ли получить водород при взаимодействии свинца с раствором серной кислоты?
 Свинец
в электрохимическом ряду находится правее водорода. В реакции замещения
способен вытеснить водород из серной кислоты, но образующийся
нерастворимый сульфат свинца прекращает доступ кислоты к металлу и
реакция прекратиться. Поэтому невозможно получить водород
взаимодействием серной кислоты и свинца. Свинец
в электрохимическом ряду находится правее водорода. В реакции замещения
способен вытеснить водород из серной кислоты, но образующийся
нерастворимый сульфат свинца прекращает доступ кислоты к металлу и
реакция прекратиться. Поэтому невозможно получить водород
взаимодействием серной кислоты и свинца.
|
Упражнение: 7
 Методом электронного баланса определите коэффициенты в уравнении реакции, схема которого: Методом электронного баланса определите коэффициенты в уравнении реакции, схема которого:
Zn + H2SO4 → ZnSO4+ H2 S↑ + H2O
Какое вещество проявляет в этой реакции восстановительные свойства?

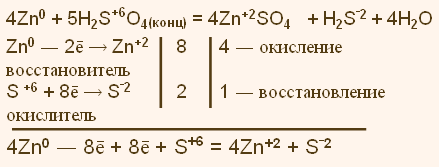
|
|